Vědci objevili, proč léky na rakovinu nefungují u všech pacientů
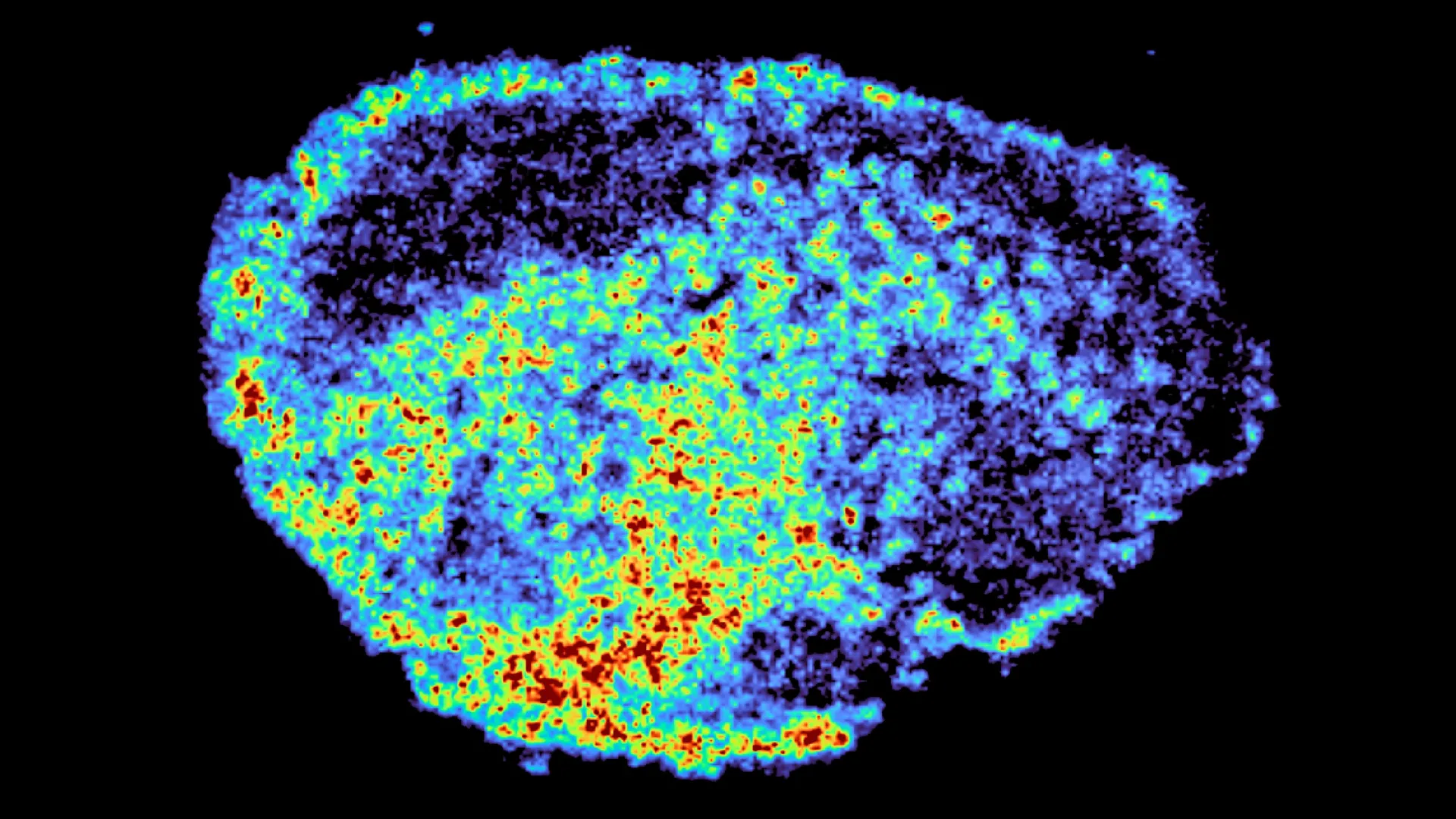
Foto: MRC Laboratory of Medical Sciences
Skrytý důvod neúčinnosti léků na rakovinu
Vědci odhalili skrytý důvod, proč léčba rakoviny nefunguje stejně dobře u všech pacientů. Některé léky se mohou zachytit uvnitř lysozomů v nádorových buňkách, kde tvoří rezervoáry s pomalým uvolňováním, což vede k nerovnoměrnému rozložení léku. To znamená, že některé rakovinné buňky jsou silně vystaveny, zatímco jiné jsou sotva ovlivněny.
Autor původního článku: redakce
Výzkum vedený Dr. Louise Fets
Studie, kterou vedla Dr. Louise Fets v MRC Laboratory of Medical Sciences a která byla publikována v časopise Nature Communications, se zaměřila na PARP inhibitory, což je třída cílených léků na rakovinu. Výzkumníci sledovali, jak se tyto léky pohybují skrze vzorky ovariálních nádorů pomocí pokročilých zobrazovacích nástrojů. Zjistili, že léky se mohou hromadit uvnitř lysozomů, malých struktur uvnitř buněk, které fungují jako „recyklační centra“. Jakmile se léky dostanou dovnitř, mohou se zachytit a později uvolnit, což ovlivňuje účinnost léčby.
Jak se léky šíří uvnitř nádorů
Možnosti léčby rakoviny se v posledních letech rychle rozšířily, což zlepšilo výsledky pro mnoho pacientů. PARP inhibitory zejména transformovaly péči o rakovinu vaječníků. Nicméně ne všichni pacienti mají prospěch a někteří si časem vyvinou rezistenci. Aby tyto léky fungovaly, musí se hromadit uvnitř rakovinných buněk v dostatečně vysokých úrovních, aby vyvolaly buněčnou smrt. Přesto vědci stále mají omezené pochopení toho, jak se léky rozdělují uvnitř nádorů a co tento proces řídí.
Výzkumníci použili tenké plátky ovariálních nádorů odebraných od pacientů a udržovaných naživu v laboratoři. Tyto vzorky, známé jako „explantáty“, byly ošetřeny PARP inhibitory, aby vědci mohli přímo pozorovat, jak se léky pohybují skrze skutečnou lidskou nádorovou tkáň. Pomocí hmotnostní spektrometrie vytvořili detailní mapy ukazující přesně, kde se léky hromadí. Spojili to s prostorovou transkriptomikou, která jim umožnila zkoumat genovou aktivitu v oblastech s vysokými a nízkými úrovněmi léků ve stejném vzorku.
Lysozomy jako skryté rezervoáry léků
Výzkumníci objevili, že lysozomy hrají klíčovou roli v této nerovnoměrné distribuci. Některé PARP inhibitory jsou vtahovány do těchto kompartmentů a ukládány tam místo toho, aby se rovnoměrně rozšířily po celé buňce. To vytváří vnitřní kapsy, kde se léky hromadí. Tyto lysozomy fungují jako rezervoáry s pomalým uvolňováním – drží lék a postupně ho uvolňují – což zvyšuje expozici v určitých buňkách, zatímco jiné zůstávají s mnohem nižšími úrovněmi.
Ne všechny PARP inhibitory se chovají stejně. Studie zjistila, že léky jako rucaparib a niraparib jsou tímto procesem ovlivněny, zatímco jiné, jako olaparib, nikoliv. „Byli jsme překvapeni velkou variabilitou v akumulaci léků na úrovni jednotlivých buněk. Tato variabilita byla způsobena hromaděním léku v lysozomech, které fungují jako rezervoáry, zvyšující expozici rakovinných buněk lékům tím, že lék ukládají a uvolňují, když je to potřeba,“ říká Dr. Carmen Ramirez Moncayo, první autorka a postdoktorandka v LMS.
Budoucnost léčby rakoviny
PARP inhibitory jsou již široce používány k léčbě rakoviny vaječníků, prsu a prostaty a jsou testovány u mnoha dalších typů rakoviny. Lepší pochopení toho, jak jsou tyto léky ukládány a distribuovány uvnitř buněk, by mohlo vést k více personalizovaným léčebným strategiím, zlepšujícím účinnost a snižujícím rezistenci a relapsy.
„Pochopením toho, jak jsou léky přijímány do buněk, můžeme pochopit, zda to ovlivňuje, proč léky na rakovinu fungují u některých lidí a u jiných ne. Nakonec doufáme, že budeme schopni studovat molekulární podpis nádoru pacienta, abychom pomohli přizpůsobit terapeutické přístupy více personalizovaným způsobem,“ říká Dr. Louise Fets, hlavní autorka a vedoucí skupiny pro transport léků a metabolismus nádorů v LMS.
Tato studie byla provedena pomocí nádorové tkáně udržované mimo tělo. U skutečných pacientů jsou léky dodávány krevním řečištěm a krevní cévy nádorů jsou často neuspořádané, což může dále přispívat k nerovnoměrné distribuci léků. Budoucí studie použijí zvířecí modely a větší skupiny pacientů, aby lépe pochopily, jak interagují dodávka léků, struktura nádoru a lysozomální ukládání v klinických podmínkách, včetně relapsujících rakovin.
Výzkum byl podpořen financováním od Medical Research Council, Cancer Research UK a dalších organizací.
Mohlo by vás zajímat
- Vědci našli imunitní buňku spojenou s únavou a příznaky dlouhého COVIDu
- Lék na hubnutí Ozempic snižuje riziko deprese, úzkosti a závislostí
- 165 000 pacientů s demencí odhaluje skryté riziko mrtvice z běžného léku
Původní článek: Scientists discover why cancer drugs don’t work for everyone